
Todo el contenido de iLive se revisa médicamente o se verifica para asegurar la mayor precisión posible.
Tenemos pautas de abastecimiento estrictas y solo estamos vinculados a sitios de medios acreditados, instituciones de investigación académica y, siempre que sea posible, estudios con revisión médica. Tenga en cuenta que los números entre paréntesis ([1], [2], etc.) son enlaces a estos estudios en los que se puede hacer clic.
Si considera que alguno de nuestros contenidos es incorrecto, está desactualizado o es cuestionable, selecciónelo y presione Ctrl + Intro.
Un sistema de administración de fármacos en bucle cerrado puede mejorar la administración de quimioterapia
Último revisado: 02.07.2025
Cuando los pacientes con cáncer se someten a quimioterapia, las dosis de la mayoría de los fármacos se calculan en función de su superficie corporal. Esto se estima mediante una ecuación que considera la altura y el peso del paciente. Esta ecuación se formuló en 1916 con base en datos de tan solo nueve pacientes.
Este enfoque simplificado de la dosificación no tiene en cuenta otros factores y puede provocar que el paciente reciba una dosis excesiva o insuficiente del fármaco. Como resultado, algunos pacientes pueden experimentar toxicidad innecesaria o una eficacia insuficiente de la quimioterapia que reciben.
Para mejorar la precisión de la dosificación de la quimioterapia, los ingenieros del MIT han desarrollado un enfoque alternativo que permite personalizar la dosis para cada paciente. Su sistema mide la cantidad de fármaco en el cuerpo del paciente y envía esos datos a un controlador que puede ajustar la velocidad de infusión según corresponda.
Este enfoque podría ayudar a compensar las diferencias en la farmacocinética de los medicamentos causadas por la composición corporal, la predisposición genética, la toxicidad orgánica inducida por la quimioterapia, las interacciones con otros medicamentos y alimentos, y las variaciones circadianas en las enzimas responsables de descomponer los medicamentos de quimioterapia, dicen los investigadores.
"Al reconocer los avances en la comprensión de cómo se metabolizan los medicamentos y aplicar herramientas de ingeniería para simplificar la dosificación personalizada, creemos que podemos ayudar a transformar la seguridad y la eficacia de muchos medicamentos", dijo Giovanni Traverso, profesor asociado de ingeniería mecánica en el MIT, gastroenterólogo en el Brigham and Women's Hospital y autor principal del estudio.
Louis DeRidder, estudiante de posgrado del MIT, es el autor principal del artículo publicado en la revista Med.
Monitoreo continuo
En este estudio, los investigadores se centraron en un fármaco llamado 5-fluorouracilo, utilizado para tratar el cáncer colorrectal y otros tipos de cáncer. El fármaco se administra generalmente durante un período de 46 horas y su dosis se determina mediante una fórmula basada en la altura y el peso del paciente, que proporciona una estimación de la superficie corporal.
Sin embargo, este enfoque no considera las diferencias en la composición corporal que pueden afectar la distribución del fármaco en el organismo, ni las variaciones genéticas que afectan su metabolismo. Estas diferencias pueden provocar efectos secundarios perjudiciales si se administra una dosis excesiva del fármaco. Si no se administra la cantidad suficiente, es posible que no destruya el tumor como se espera.
"Las personas con la misma superficie corporal pueden tener alturas y pesos muy diferentes, distinta masa muscular o distinta genética, pero siempre que la altura y el peso introducidos en esa ecuación den como resultado la misma superficie corporal, su dosis es idéntica", afirma DeRidder, candidato a doctorado en el programa de ingeniería médica y física médica del Programa de Ciencias de la Salud y Tecnología de Harvard-MIT.
Otro factor que puede alterar la cantidad de fármaco en la sangre en un momento dado es la variación circadiana de una enzima llamada dihidropirimidina deshidrogenasa (DPD), que descompone el 5-fluorouracilo. La expresión de DPD, al igual que la de muchas otras enzimas del organismo, está regulada por un ritmo circadiano. Por lo tanto, la degradación del 5-FU por DPD no es constante, sino que varía con la hora del día. Estos ritmos circadianos pueden resultar en una variación de diez veces en la cantidad de 5-FU en la sangre de un paciente durante una infusión.
Al utilizar la superficie corporal para calcular la dosis de quimioterapia, sabemos que dos personas pueden presentar toxicidades muy diferentes a causa del 5-fluorouracilo. Un paciente puede tener ciclos de tratamiento con una toxicidad mínima y luego un ciclo con una toxicidad grave. Algo ha cambiado en la forma en que el paciente metaboliza la quimioterapia de un ciclo al siguiente. Nuestro método de dosificación obsoleto no refleja estos cambios, y los pacientes sufren las consecuencias, afirma Douglas Rubinson, oncólogo clínico del Instituto de Cáncer Dana-Farber y autor del artículo.
Una forma de intentar compensar la variabilidad en la farmacocinética de la quimioterapia es una estrategia llamada monitorización farmacoterapéutica, en la que el paciente proporciona una muestra de sangre al final de un ciclo de tratamiento. Tras analizar esta muestra para determinar las concentraciones del fármaco, la dosis puede ajustarse, si es necesario, al inicio del siguiente ciclo (normalmente dos semanas para el 5-fluorouracilo).
Se ha demostrado que este enfoque produce mejores resultados para los pacientes, pero no se ha utilizado ampliamente para quimioterapias como el 5-fluorouracilo.
Los investigadores del MIT querían desarrollar un tipo de monitorización similar, pero de forma automatizada, que permitiera personalizar la dosificación de los medicamentos en tiempo real, lo que podría conducir a mejores resultados para los pacientes.
En su sistema de circuito cerrado, las concentraciones del fármaco se pueden monitorear continuamente y esta información se utiliza para ajustar automáticamente la velocidad de infusión del fármaco de quimioterapia para mantener la dosis dentro del rango objetivo.
Este sistema de circuito cerrado permite personalizar la dosificación de medicamentos para tener en cuenta los ritmos circadianos de los niveles de enzimas metabolizadoras de medicamentos, así como cualquier cambio en la farmacocinética del paciente desde el último tratamiento, como la toxicidad orgánica inducida por la quimioterapia.
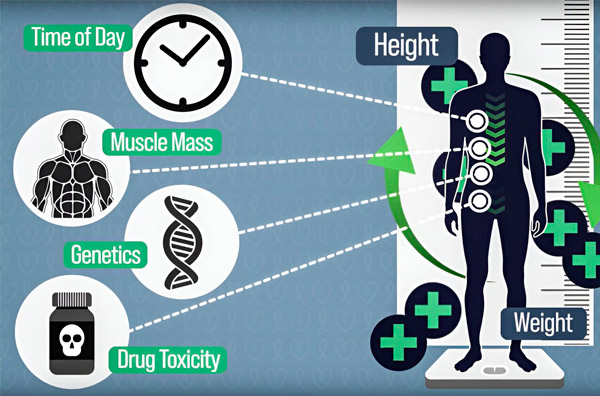
Para aumentar la precisión en la dosificación de la quimioterapia, ingenieros del MIT han desarrollado un método para medir continuamente la cantidad de fármaco en el cuerpo del paciente durante una infusión de varias horas. Esto ayudará a compensar las diferencias causadas por la composición corporal, la genética, la toxicidad de los fármacos y las oscilaciones circadianas. Fuente: Cortesía de los investigadores.
El nuevo sistema desarrollado por los investigadores, conocido como CLAUDIA (Regulador Automático de Infusión de Medicamentos de Circuito Cerrado), utiliza equipos disponibles comercialmente en cada paso. Se toman muestras de sangre cada cinco minutos y se preparan rápidamente para su análisis. Se mide la concentración de 5-fluorouracilo en sangre y se compara con el rango objetivo.
La diferencia entre las concentraciones objetivo y medidas se ingresa en un algoritmo de control, que luego ajusta la velocidad de infusión según sea necesario para mantener la dosis dentro del rango de concentraciones en las que el medicamento es efectivo y no tóxico.
"Hemos desarrollado un sistema que nos permite medir continuamente la concentración del fármaco y ajustar la velocidad de infusión en consecuencia para mantener la concentración del fármaco dentro de la ventana terapéutica", afirma DeRidder.
Ajuste rápido
En pruebas con animales, los investigadores descubrieron que usando CLAUDIA podían mantener la cantidad de medicamento circulante en el cuerpo dentro del rango objetivo aproximadamente el 45 por ciento del tiempo.
Los niveles del fármaco en animales que recibieron quimioterapia sin CLAUDIA se mantuvieron dentro del rango objetivo solo un 13 % del tiempo en promedio. Los investigadores no evaluaron la eficacia de los niveles del fármaco en este estudio, pero se cree que mantener las concentraciones dentro del rango objetivo produce mejores resultados y menor toxicidad.
CLAUDIA también logró mantener la dosis de 5-fluorouracilo dentro del rango objetivo, incluso al administrar un fármaco inhibidor de la enzima DPD. En animales que recibieron este inhibidor sin monitorización ni ajuste continuos, los niveles de 5-fluorouracilo aumentaron hasta ocho veces.
Para esta demostración, los investigadores realizaron manualmente cada paso del proceso utilizando equipos disponibles comercialmente, pero ahora planean automatizar cada paso para que el monitoreo y los ajustes de dosis se puedan realizar sin intervención humana.
Para medir las concentraciones del fármaco, los investigadores utilizaron cromatografía líquida de alto rendimiento-espectrometría de masas (HPLC-MS), una técnica que puede adaptarse para detectar casi cualquier tipo de fármaco.
"Vemos un futuro en el que podremos utilizar CLAUDIA para cualquier fármaco que tenga las propiedades farmacocinéticas adecuadas y sea detectable por HPLC-MS, lo que permitirá una dosificación personalizada para muchos fármacos diferentes", afirma DeRidder.
