
Todo el contenido de iLive se revisa médicamente o se verifica para asegurar la mayor precisión posible.
Tenemos pautas de abastecimiento estrictas y solo estamos vinculados a sitios de medios acreditados, instituciones de investigación académica y, siempre que sea posible, estudios con revisión médica. Tenga en cuenta que los números entre paréntesis ([1], [2], etc.) son enlaces a estos estudios en los que se puede hacer clic.
Si considera que alguno de nuestros contenidos es incorrecto, está desactualizado o es cuestionable, selecciónelo y presione Ctrl + Intro.
Acinesia miocárdica
Médico experto del artículo.
Último revisado: 04.07.2025
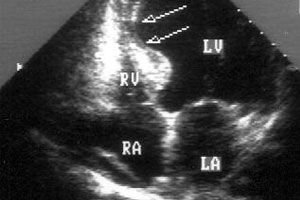
Al diagnosticar enfermedades cardíacas se puede detectar la acinesia miocárdica, es decir, su inmovilidad o la incapacidad de determinadas zonas del tejido muscular del corazón para contraerse.
Por lo tanto, la acinesia miocárdica no es una enfermedad, sino un estado patológico, un trastorno de la función motora normal del músculo cardíaco, que se determina mediante diagnóstico por ultrasonido del corazón y es uno de los signos estructurales y funcionales de una serie de enfermedades del sistema cardiovascular.
Causas acinesia miocárdica
¿Por qué el músculo cardíaco deja de contraerse, es decir, cuáles son las causas de la acinesia miocárdica?
En la práctica cardiológica, la patogénesis de la pérdida de la función contráctil normal del miocardio (que, como es sabido, se realiza automáticamente en un corazón sano) se asocia con mayor frecuencia al infarto de miocardio y la consiguiente necrosis de parte de los cardiomiocitos funcionales. Los cambios reparativos (remodelación) del miocardio postinfarto conducen primero a un aumento en la zona de infarto, y posteriormente a la distorsión y expansión de la forma del ventrículo, transformándose la zona de necrosis de los cardiomiocitos en una cicatriz y formando una región de acinesia miocárdica. Los cambios fibrosos también pueden afectar el tabique que separa los ventrículos, y entonces la ecografía muestra acinesia en la zona del tabique interventricular.
El infarto de miocardio es un estado agudo de isquemia cardíaca o enfermedad cardíaca isquémica (ECI), que se desarrolla cuando se altera la circulación sanguínea en el sistema de la arteria coronaria, lo que conduce a la hipoxia miocárdica y a la muerte de sus células.
En caso de adelgazamiento postinfarto de la zona de la membrana muscular del corazón y su protrusión (aneurisma), la cardiografía ecográfica revela acinesia del ventrículo izquierdo. En casi dos tercios de los pacientes, la formación de un aneurisma se produce en el ventrículo izquierdo, en su pared anterior o en el ápice, y en este caso también se observa acinesia del ápice cardíaco.
Además, existe una correlación entre los resultados ecocardiográficos que visualizan la acinesia miocárdica y el síndrome miocárdico postinfarto: cardiosclerosis postinfarto focal o difusa con reemplazo característico de cardiomiocitos dañados por tejido fibroso, así como con daño al sistema de conducción cardíaca (conducción deteriorada de impulsos bioeléctricos por células de los nódulos sinoauriculares o auriculoventriculares).
En los casos de degeneración o distrofia miocárdica, que tiene un cuadro histomorfológico similar a la cardiosclerosis, los cambios en la estructura del tejido muscular cardíaco también demuestran acinesia miocárdica focal.
A menudo hay daños a las células del nódulo sinoatrial con una disminución en la amplitud del movimiento de la pared muscular y la ausencia de su contracción, es decir, una combinación de hipocinesia y acinesia en pacientes con miocarditis infecciosa. Esta enfermedad puede estar acompañada por la formación de infiltrados inflamatorios en el intersticio y miocitolisis localizada debido a la inflamación causada por virus (adeno y enterovirus, Picornaviridae, virus Coxsackie, Parvovirus B, virus de la rubéola, HSV-6), bacterias (Corynebacterium diphtheriae, Haemophilus influenzae, Borrelia burgdorferi, Mycoplasma pneumoniae), así como protozoos (Trypanosoma cruzi, Toxoplasma gondii), hongos (Aspergillus) o parásitos (Ascaris, Echinococcus granulosus, Paragonimus westermani, etc.). Según muestran las estadísticas clínicas, la mayoría de los casos de miocarditis infecciosa son causados por difteria, influenza, enterovirus y toxoplasma.
Y en la miocarditis de etiología autoinmune (asociada a lupus eritematoso sistémico, esclerodermia, artritis reumatoide, enfermedad de Whipple, etc.) puede producirse acinesia del ventrículo izquierdo y su disfunción, plagada de arritmias potencialmente mortales.
Por otra parte, los cardiólogos distinguen la miocardiopatía por estrés (miocardiopatía de Takotsubo), que los especialistas locales denominan síndrome del corazón roto. Esta disfunción sistólica transitoria y repentina de los segmentos medioapical del ventrículo izquierdo suele presentarse en situaciones de estrés en mujeres mayores sin antecedentes de enfermedad coronaria. En particular, se detecta una zona de hipercinesia en la base del ventrículo izquierdo y, por encima de ella, acinesia del ápex cardíaco. Además, en la ecografía cardíaca, se puede detectar una falta de movimiento en la zona del tabique interventricular.
Factores de riesgo
Los principales factores de riesgo para los trastornos de la función motora normal de las áreas del músculo cardíaco, en forma de acinesia miocárdica, son el desarrollo de cardiopatía isquémica. Los factores de riesgo para su desarrollo se consideran, a su vez, los siguientes:
- edad mayor de 45 años para los hombres y mayor de 55 años para las mujeres;
- Antecedentes familiares de enfermedad cardíaca temprana;
- reducción de los niveles de HDL (lipoproteínas de alta densidad) transportadoras de colesterol en la sangre y aumento de los niveles de lipoproteínas de baja densidad (LDL), que contribuyen a la deposición de colesterol en las paredes de los vasos sanguíneos – aterosclerosis;
- niveles altos de triglicéridos en la sangre (relacionados con la dieta);
- hipertensión;
- trastorno metabólico (síndrome metabólico) que contribuye al aumento de la presión arterial y al depósito de colesterol en los vasos coronarios;
- tabaquismo (incluido el tabaquismo pasivo), obesidad, falta de actividad física, estrés psicológico y depresión.
Las infecciones virales y bacterianas que afectan al miocardio, así como las patologías autoinmunes, desencadenan un factor de riesgo de isquemia miocárdica como el aumento de la concentración de proteína C reactiva (PCR) en sangre. El estado normal de los vasos cardíacos se ve alterado por un desequilibrio de los activadores tisulares del plasminógeno (tPA) y sus inhibidores (PAI), lo que supone un riesgo de trombosis de las venas coronarias con su oclusión completa.
Patogenesia
Se sugiere que la patogenia de esta miocardiopatía radica en la respuesta inadecuada de los vasos cardíacos (arterias coronarias y/o arteriolas y capilares) a la liberación de neurotransmisores catecolaminas a la sangre, y que las anormalidades a corto plazo en la contracción miocárdica surgen debido al vasoespasmo que provocan.
Síntomas acinesia miocárdica
En caso de acinesia miocárdica (un signo ecocardiográfico de enfermedades cardiovasculares), el cuadro clínico se determina por los síntomas de estas patologías. Entre ellos se encuentran: disnea, dolor de intensidad variable en la zona cardíaca, arritmia (auricular o ventricular), aleteo ventricular y desmayos.
Así, en la miocardiopatía de takotsubo los pacientes se quejan con mayor frecuencia de dolor detrás del esternón (de naturaleza opresiva) que se irradia al omóplato izquierdo y una sensación de falta de aire al inhalar.
Los dolores de la miocarditis pueden ser agudos y prolongados (sin efecto con el uso de nitroglicerina) y sordos (opresivos). Además, los síntomas cardíacos en esta enfermedad de origen infeccioso incluyen disnea, fiebre, aumento de la frecuencia cardíaca y aleteo cardíaco; también pueden presentarse alteraciones hemodinámicas fulminantes (disminución de la velocidad del flujo sanguíneo), pérdida del conocimiento y muerte súbita cardíaca.
Complicaciones y consecuencias
Ciertamente, la acinesia miocárdica, en comparación con la discinesia de la zona cicatricial postinfarto, representa un peligro más grave para la vida de los pacientes con infarto de miocardio. Estudios han demostrado que, en aproximadamente el 40 % de los casos de infarto con obstrucción de vasos coronarios, con la restauración oportuna del flujo sanguíneo en el segmento isquémico (reperfusión), la contractilidad miocárdica se restablece entre dos y seis semanas después del infarto. Sin embargo, sus consecuencias y complicaciones incluyen taponamiento cardíaco repentino, disociación electromecánica y muerte.
Las consecuencias y complicaciones de los cambios distróficos en el miocardio con su acinesia parcial conducen a la atrofia casi inevitable de las fibras musculares, que puede manifestarse no solo como arritmia y una disminución de la eyección sistólica, sino también como una expansión de las cámaras del corazón con insuficiencia circulatoria crónica.
La acinesia ventricular izquierda con su disfunción sistólica e insuficiencia cardíaca se encuentra entre los predictores más fuertes del riesgo de muerte cardíaca súbita.
 [ 23 ]
[ 23 ]
Diagnostico acinesia miocárdica
Sólo el diagnóstico instrumental del miocardio mediante el examen ecográfico del corazón ( ecocardiografía ) permite detectar zonas de acinesia.
Un método especial de análisis segmentario automático de las contracciones cardíacas permite rastrear y registrar todos los movimientos de la pared del corazón.
¿Qué es necesario examinar?
Diagnóstico diferencial
El diagnóstico diferencial del dolor torácico en pacientes con un cuadro clínico atípico o con resultados de electrocardiograma diagnósticamente indeterminados también implica el uso de la ecocardiografía.
En pacientes sin trastorno del movimiento miocárdico, la ecocardiografía se puede utilizar para detectar otras afecciones potencialmente mortales con un cuadro clínico similar: embolia pulmonar masiva o disección aórtica.
Además, el diagnóstico del miocardio, incluso en casos de trastornos de su función contráctil, incluye análisis de sangre para determinar la VSG, los niveles de proteína C reactiva, anticuerpos (análisis serológico del suero para los niveles de IgM), los niveles de electrolitos y la determinación de marcadores de daño miocárdico (isoenzimas de troponina I y T, creatina quinasa).
Los pacientes se someten a un electrocardiograma (ECG), una angiografía coronaria con contraste de rayos X, una gammagrafía tomográfica (con radioisótopos), un Doppler tisular color y una resonancia magnética. El diagnóstico de aneurismas cardíacos requiere la ventriculografía con contraste de rayos X.
En algunos casos, el diagnóstico diferencial del miocardio sólo es posible con la ayuda de una biopsia endomiocárdica seguida de la histología de la muestra obtenida.
¿A quién contactar?
Tratamiento acinesia miocárdica
El tratamiento del miocardio tiene como objetivo restablecer el suministro de sangre a sus zonas dañadas (perfusión) y su función de conducción, limitar el área de necrosis localizada de los cardiomiocitos y activar el metabolismo celular.
En la práctica clínica, se utilizan fármacos de diversos grupos farmacológicos. En los síndromes coronarios agudos y la trombosis oclusiva de la arteria coronaria epicárdica, la terapia de reperfusión se realiza con fármacos trombolíticos (estreptoquinasa, prouroquinasa, alteplasa) y antiagregantes plaquetarios (ticlopidina, sulfato de clopidogrel o Plavix).
En la insuficiencia cardíaca crónica, se utilizan fármacos que inhiben la enzima convertidora de angiotensina (ECA) que regula la presión arterial: captopril, enalapril, ramipril, fosinopril. Su dosis la determina un cardiólogo según la enfermedad específica y las lecturas del ECG. Por ejemplo, el captopril (Capril, Alopresin, Tensiomin) se puede recetar en dosis de 12,5 a 25 mg, tres veces al día antes de las comidas (por vía oral o sublingual). Los efectos secundarios de este fármaco y de la mayoría de los fármacos de este grupo incluyen taquicardia, descenso de la presión arterial, disfunción renal, insuficiencia hepática, náuseas y vómitos, diarrea, urticaria, aumento de la ansiedad, insomnio, parestesia y temblor, y cambios en la composición bioquímica de la sangre (incluida la leucopenia). Hay que tener en cuenta que los inhibidores de la ECA no se utilizan en casos de patologías miocárdicas idiopáticas, hipertensión arterial, estenosis de la aorta y de los vasos renales, cambios hiperplásicos en la corteza suprarrenal, ascitis, embarazo y infancia.
En caso de cardiopatía coronaria y miocardiopatía, se pueden recetar fármacos antiisquémicos vasodilatadores periféricos, como molsidomina (Motazomine, Corvaton, Sidnofarm) o Advocard. La molsidomina se administra por vía oral: un comprimido (2 mg) tres veces al día. Está contraindicada en caso de hipotensión y shock cardiogénico. Su efecto secundario es cefalea.
El verapamilo (Veracard, Lekoptin), un fármaco antiarrítmico e hipotensor, se utiliza para la cardiopatía coronaria con taquicardia y angina de pecho: un comprimido (80 mg) tres veces al día. Puede presentar efectos secundarios como náuseas, sequedad bucal, problemas intestinales, dolor de cabeza y muscular, insomnio, urticaria y alteraciones de la frecuencia cardíaca. Este fármaco está contraindicado en casos de insuficiencia cardíaca grave, fibrilación auricular, bradicardia e hipotensión.
El medicamento Mildronate (Meldonium, Angiocardil, Vasonate, Cardionate y otras marcas comerciales) tiene un efecto cardiotónico y antihipóxico. Se recomienda tomar una cápsula (250 mg) dos veces al día. Este medicamento solo puede ser utilizado por adultos y está contraindicado en casos de trastornos de la circulación cerebral y patologías estructurales del cerebro. Al usar Mildronate, pueden presentarse efectos secundarios como dolor de cabeza, mareos, arritmia cardíaca, dificultad para respirar, sequedad bucal, tos, náuseas y trastornos intestinales.
Los fármacos del grupo de los β1-adrenobloqueantes para la enfermedad coronaria (metoprolol, propranolol, atenolol, acebutolol, etc.) reducen principalmente la presión arterial y, al reducir la estimulación simpática de los receptores en las membranas celulares del miocardio, reducen la frecuencia cardíaca y el gasto cardíaco, lo que aumenta el consumo de oxígeno por los cardiomiocitos y alivia el dolor. Por ejemplo, el metoprolol se prescribe en un comprimido dos veces al día, mientras que el atenolol es suficiente con un comprimido al día. Sin embargo, los fármacos de este grupo aumentan el riesgo de insuficiencia cardíaca aguda y bloqueo auricular y ventricular, y su uso está contraindicado en presencia de insuficiencia cardíaca congestiva y descompensada, bradicardia y trastornos circulatorios. Por lo tanto, muchos expertos cuestionan actualmente el efecto antiarrítmico de estos fármacos.
Aliviar el dolor cardíaco es fundamental, ya que la activación simpática durante el dolor provoca la constricción de los vasos sanguíneos y aumenta la carga sobre el corazón. La nitroglicerina se usa comúnmente para aliviar el dolor. Información detallada en el artículo: Pastillas efectivas para aliviar el dolor cardíaco.
Los médicos recomiendan tomar vitaminas B6, B9, E y, para apoyar el sistema de conducción cardíaca, medicamentos que contengan potasio y manganeso (Panangin, Asparkam, etc.).
Tratamiento quirúrgico
En casos de infartos con daño a las arterias coronarias (que conduce a la formación de una zona de isquemia miocárdica y su acinesia con expansión de las cámaras del corazón), está indicado el tratamiento quirúrgico para restablecer el flujo sanguíneo al corazón: bypass aortocoronario.
En caso de cardiopatía isquémica, se utiliza la dilatación coronaria (expansión de la luz) – colocación de stents.
El tratamiento más frecuentemente utilizado para los aneurismas discinéticos es el quirúrgico: ya sea mediante aneurismectomía (resección), suturando la cavidad aneurismática (aneurismoplastia) o reforzando su pared.
Se ha desarrollado un método de cardiomioplastia dinámica que consiste en restaurar o mejorar la contractilidad miocárdica mediante músculo esquelético electroestimulado (generalmente un colgajo del borde del dorsal ancho) que envuelve una parte del corazón (con resección parcial de la segunda costilla). El colgajo muscular se sutura alrededor de los ventrículos y su estimulación sincronizada con las contracciones cardíacas se realiza mediante electrodos intramusculares de un marcapasos cardíaco implantable.
Prevención
Regrese a la sección de Factores de Riesgo y verá claramente cómo prevenir las patologías cardiovasculares. Lo principal es no subir de peso, moverse más y evitar que el colesterol se acumule en forma de placas en las paredes de los vasos sanguíneos. Para ello, es útil después de los 40 años (y ante la presencia de patologías cardíacas en familiares consanguíneos) seguir la Dieta para la Aterosclerosis.
Y, por supuesto, los cardiólogos consideran que dejar de fumar es la condición más importante para prevenir el daño isquémico al miocardio. Al fumar, las proteínas de hemoglobina de los glóbulos rojos se combinan con los gases del humo del tabaco inhalado, formando un compuesto muy perjudicial para el corazón: la carboxihemoglobina. Esta sustancia impide que las células sanguíneas transporten oxígeno, lo que provoca hipoxia de los cardiomiocitos del músculo cardíaco y el desarrollo de isquemia miocárdica.
Lea también: Prevención de la cardiosclerosis postinfarto
Pronóstico
Los cardiólogos se muestran reacios a proporcionar información pronóstica: es difícil hacer un pronóstico preciso de la discinesia, hipocinesia y acinesia postinfarto.
Para evaluar el pronóstico de mortalidad tras un infarto agudo de miocardio, expertos de la Sociedad Americana de Ecocardiografía introdujeron el Índice de Movimiento de la Pared (IMP). Sin embargo, este no tiene un valor pronóstico completo a largo plazo.
En cuanto a la miocarditis, según las estadísticas, casi el 30% de los casos se curan, y en el resto, la disfunción crónica del ventrículo izquierdo se convierte en una complicación. Además, alrededor del 10% de los casos de miocarditis viral y microbiana provocan la muerte de los pacientes. La acinesia total del miocardio provoca un paro cardíaco.

