
Todo el contenido de iLive se revisa médicamente o se verifica para asegurar la mayor precisión posible.
Tenemos pautas de abastecimiento estrictas y solo estamos vinculados a sitios de medios acreditados, instituciones de investigación académica y, siempre que sea posible, estudios con revisión médica. Tenga en cuenta que los números entre paréntesis ([1], [2], etc.) son enlaces a estos estudios en los que se puede hacer clic.
Si considera que alguno de nuestros contenidos es incorrecto, está desactualizado o es cuestionable, selecciónelo y presione Ctrl + Intro.
Neuroprótesis para el tracto gastrointestinal: restaura el peristaltismo y activa las hormonas de la saciedad.
Último revisado: 18.08.2025
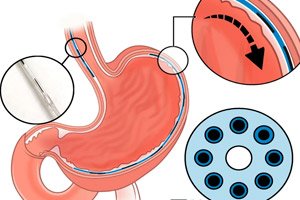 ">
">Los trastornos de la motilidad gastrointestinal (esófago y estómago) —acalasia, gastroparesia, disfagia, etc.— afectan a más del 20% de la población y causan una morbilidad y unos costes considerables. Los tratamientos habituales —medicamentos, intervenciones conductuales y cirugía— suelen tener una eficacia limitada y no logran restablecer la peristalsis coordinada.
- Por qué los dispositivos existentes no resuelven el problema. La estimulación eléctrica del tracto gastrointestinal se ha estudiado desde la década de 1960, pero los implantes clínicamente aprobados (p. ej., Enterra para la gastroparesia, estimuladores vagales VBLOC para la obesidad, estimulación sacra InterStim para la incontinencia fecal) funcionan principalmente en un circuito abierto y a menudo producen efectos inconsistentes en el vaciamiento gástrico. Esto se debe a que una o más fuentes de corriente con parámetros constantes no reproducen la complejidad espaciotemporal de la peristalsis natural.
- Fisiología que debe ser imitada. La peristalsis es un circuito cerrado: señales sensoriales (estiramiento, temperatura, estímulos químicos) → respuestas reflejas en el plexo mientérico y el músculo liso. Además del transporte de alimentos, la motilidad afecta las señales aferentes intestino-cerebro y las hormonas de la saciedad (GLP-1, insulina, grelina), lo que genera apetito y sensación de saciedad. En la dismotilidad, estos circuitos se interrumpen.
- Brecha tecnológica. Para reproducir las ondas correctas, se requiere estimulación multicanal directamente cerca del plexo mientérico y la capa muscular. Sin embargo, el acceso a estas zonas suele requerir cirugía invasiva; las técnicas endoscópicas avanzadas (p. ej., NOTES) son complejas y su uso no está extendido. Se requieren instrumentos mínimamente invasivos que permitan la colocación precisa de electrodos en la submucosa y funcionen en un circuito cerrado de detección y estimulación.
- Lo que ofrece el nuevo trabajo. Los autores describen una neuroprótesis multicanal, instalada endoscópicamente y con estimulación eléctrica y química, capaz de activar ondas peristálticas coordinadas al recibir una señal sobre el paso de un bolo. Esto no solo restaura la motilidad, sino que también modula la respuesta metabólica (acercándola a un estado de "alimentación"). Esto cubre deficiencias clave: acceso a la capa deseada, coordinación espaciotemporal y trabajo en circuito cerrado.
En resumen: existe un amplio nicho clínico: desmotivaciones generalizadas y mal tratadas. Los estímulos "abiertos" anteriores no imitan la fisiología natural. Por lo tanto, es lógico intentar enseñar al implante a "pensar como el tracto gastrointestinal": detectar el bolo alimenticio y activar la peristalsis fisiológica exactamente donde pasa la señal natural: en el plexo mientérico.
Un equipo del MIT, Harvard y Brigham creó un implante esofágico/gástrico en miniatura que detecta el bolo alimenticio en un circuito cerrado y desencadena ondas coordinadas de peristalsis. En cerdos, el dispositivo no solo restauró la motilidad esofágica y gástrica, sino que también indujo cambios hormonales similares a los del estado posprandial (tras la comida). El implante se coloca por vía endoscópica, sin cirugía abdominal. El estudio se publicó en la revista Nature.
¿Qué se les ocurrió?
- El implante. Una neuroprótesis fibrosa delgada de ≈1,25 mm de diámetro con siete electrodos cada 1 cm y un microcanal para la administración local de sustancias (electroestimulación y quimioestimulación). Su flexibilidad y dimensiones permiten su inserción a través del canal instrumental estándar de un endoscopio (2,8-3,2 mm).
- Instalación. Se ha desarrollado un instrumento endoscópico: una aguja con un gancho de nitinol de tracción inversa, hidrodisección y la clave: la búsqueda de la submucosa mediante impedancia tisular para una colocación precisa justo por encima de la capa muscular, cerca del plexo mientérico.
- Circuito cerrado. El sistema lee la señal del bolo (EMG/sensores intraluminales) y selecciona un patrón de estimulación para inducir contracciones secuenciales similares a la peristalsis natural. Es posible combinar estímulos excitatorios e inhibidores, así como relajar localmente los esfínteres con microdosis de fármacos.
Lo que se mostró en los animales
- Esófago: El implante produjo "ondas de deglución" sin deglución real, incluida la relajación controlada del esfínter esofágico inferior (a través de una microadministración de glucagón) y ondas progresivas/retrógradas programables, esencialmente una "palanca de mando" peristáltica.
- Estómago. Tras 20 minutos de estimulación, la frecuencia del peristaltismo aumentó aproximadamente el doble en comparación con el grupo control (n≈4, p<0,05).
- Ilusión metabólica de saciedad. En ayunas, una estimulación de 30 minutos (esófago o estómago) provocó cambios hormonales: aumento de GLP-1 e insulina, disminución de grelina (hormona del apetito); con la estimulación gástrica, también se observó un aumento de glucagón. El perfil en general se asemejó al estado posprandial.
Detalles de seguridad e ingeniería
Pruebas breves de biocompatibilidad in vitro (extractos de material) no mostraron toxicidad; in vivo, 7 días después de la implantación: extensibilidad normal de la pared y ausencia de migración del dispositivo o daño tisular significativo. (Para mayor durabilidad y fiabilidad se requieren pruebas a largo plazo).
¿Por qué es esto necesario?
- Dismotilidad y afecciones refractarias. Acalasia, gastroparesia, disfagia, trastornos postoperatorios, donde los fármacos o intervenciones convencionales suelen tener un efecto incompleto. La estimulación local multicanal se acerca más a la fisiología real que los implantes monocanal de circuito abierto existentes.
- Trastornos metabólicos. Al controlar las vías aferentes intestino-cerebro, el dispositivo podría modular el apetito y el metabolismo, lo cual resulta interesante en el tratamiento de la obesidad y la diabetes (hipótesis hasta el momento, sin evidencia en humanos).
Limitaciones y qué sigue
Este es un trabajo preclínico en cerdos, en fase aguda-subaguda. Se realizarán estudios a largo plazo sobre la estabilidad del contacto, el aporte energético, el riesgo de fibrosis, protocolos de estimulación precisos y, posteriormente, ensayos clínicos iniciales en pacientes con formas graves de dismotividad. Sin embargo, ya se ha demostrado que la peristalsis puede activarse mediante una orden y que las respuestas hormonales pueden modificarse hacia la saciedad, todo mediante acceso endoscópico.
